鼻研究グループ
ILC2
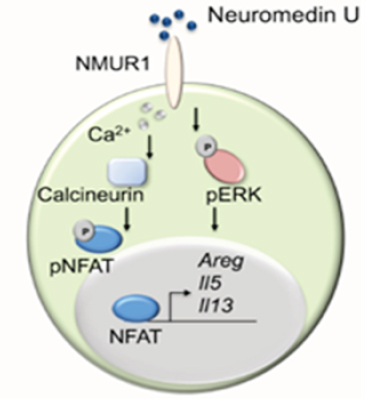
Fig.1 下気道におけるILC-2とニューロメジン(Cardoso et al. p.277-281 Nature2017より一部改変)
鼻研究グループでは好酸球性副鼻腔炎に関する研究を行っております。好酸球性副鼻腔炎は高度の鼻閉と嗅覚障害を起こす難治性かつ再発性の副鼻腔炎であり、難病指定されています。治療法として手術・経口ステロイドのほかに近年、生物学的製剤(抗IL-4/13受容体抗体)が使用されるようになりました。抗IL-4/13受容体抗体の有効性は高いのですが、抗体医薬であるため非常に高額かつ対症療法のため継続投与が必要となります。そのため、好酸球性副鼻腔炎において安価な治療薬の開発は重要な課題です。
そこで、本研究グループではニューロメジン(NMU)という神経ペプチドに着目しました。ニューロメジンU(NMU)の受容体は、好酸球性副鼻腔炎を含めたアレルギー疾患の難治に関連すると考えられている2型自然リンパ球(ILC-2)に発現があり、喘息などの呼吸器領域ではその関与が報告されており、治療ターゲットとして有用な可能性があります。ヒトニューロメジンアンタゴニスト(受容体をブロックする化合物)は京都薬科大学の高山准教授によって開発中であり、これは中分子のペプチド化合物であるため、抗体医薬と比較して安価に製剤化できます。われわれは高山准教授らと共同で好酸球性副鼻腔炎におけるNMUの機能解析を行い、ニューロメジンアンタゴニストが新規治療薬となるか研究しています。
好酸球性副鼻腔炎に対する治療は手術、経口ステロイド、抗体医薬のいずれも一長一短であり、特に薬物療法はその傾向が強く、安価だが副作用の強いステロイドと効果は高いが高価な抗体医薬の選択になっています。その中で高山准教授によるNMUR1アンタゴニストが中分子のペプチド化合物であることは大変重要であると考えています。医薬品を分子量で分類すると、一般的な医薬品である低分子医薬品、ペプチド化合物に代表される中分子医薬品、抗体医薬に代表される高分子医薬品の3種に分けられます。ステロイドを含めた低分子医薬品は化学合成されるため、製造コスト・薬価が安価である反面、オフターゲットによる副作用が多くなります。一方、抗体医薬のような高分子医薬品は標的分子への特異性が高く、難治性疾患への治療効果が期待できますが、タンパク質のため経口投与ができず細胞で合成されるため、製造コスト・薬価が極めて高額となります。中分子医薬品は両者の中間に位置し、ターゲットに対する特異性は高めで副作用が少なく、製造コストも低く抑えられ、両者の利点を兼ね備えていると思われます(舛屋 p.322-328日薬理2016)(表1)。
表1 分子量により分類した医薬品の特徴
| 低分子医薬品 | 古典的ペプチド医薬品 | 特殊環状ペプチド医薬品 | 高分子医薬品 | |
|---|---|---|---|---|
| 分子量 | 100以下 | 500〜600 | 600〜2500 | 15000以上 |
| 活性 | 高い〜普通 | 高い〜 極めて高い |
極めて高い | 極めて高い |
| 特異性 | 低い | 高い | 極めて高い | 極めて高い |
| 血中安定性 | 低い〜普通 | 極めて低い〜低い | 普通〜高い | 極めて高い |
| 経口投与 | 可能 | ほぼ不可能 | 可能 | 不可能 |
| 毒性・副作用 | 多い | 少ない | 少ない | 少ない |
| 製造コスト | 低い | 低い〜普通 | 低い〜普通 | 高い |
過去に当施設で行った好酸球性副鼻腔炎患者の手術検体を用いてNMUR1の免疫染色を行ったところ、鼻ポリープ組織の粘膜下の細胞にNMUR1の発現を確認できました。
また、好酸球数が多いと再発率が高いと言われていますが、好酸球数とNMUR1陽性細胞数との関連を調査したところ、表2のように好酸球数が多い検体ではNMUR1陽性細胞数が多く認められました(Fig.2、表2)。
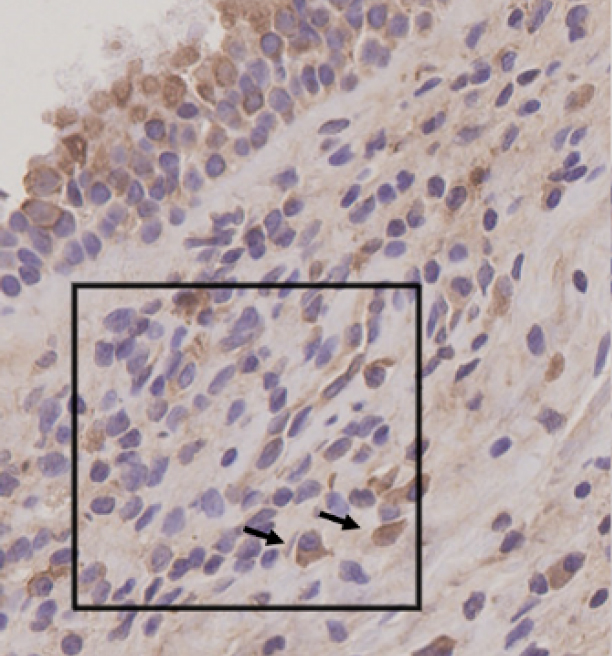
好酸球数の少ない検体
好酸球数の多い検体
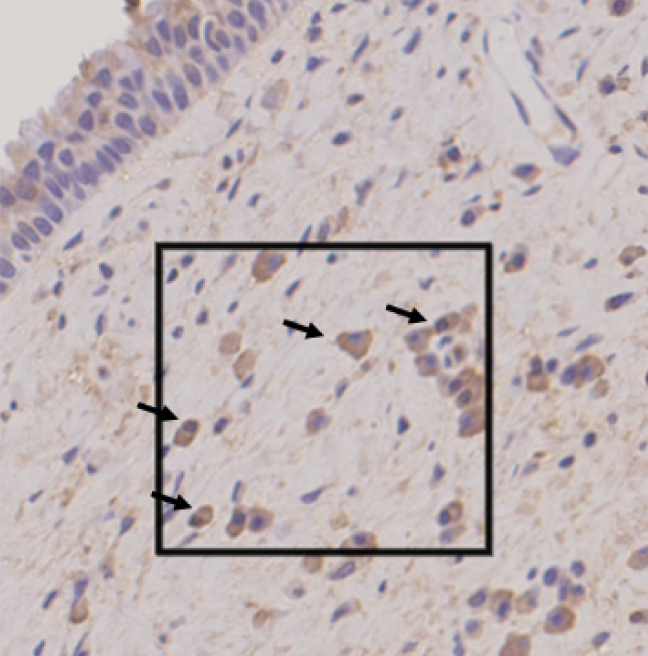
Fig.2 NMUR1による鼻ポリープ組織の免疫染色
表2 好酸球数とNMER1陽性細胞数
| 1か所目 | 2か所目 | 3か所目 | 平均 | ||
|---|---|---|---|---|---|
| 好酸球数 9個の検体 |
NMUR1陽性細胞数(A) | 14 | 9 | 8 | 10.3 |
| 全細胞数(B) | 96 | 76 | 71 | 81 | |
| 割合(%)(A/B) | 14.6 | 11.8 | 11.3 | 12.8 | |
| 好酸球数 233個の検体 |
NMUR1陽性細胞数(A) | 19 | 24 | 14 | 19 |
| 全細胞数(B) | 78 | 44 | 62 | 61.3 | |
| 割合(%)(A/B) | 24.4 | 54.5 | 22.6 | 31.0 | |
- ■好酸球数233個の検体のNMUR1陽性細胞数(A)の平均は、好酸球数9個の検体のNMUR1陽性細胞数(A)の平均の約2倍
- ■好酸球数233個の検体の割合(%)(A/B)の平均は、好酸球数9個の検体の割合(%)(A/B)の平均の約3倍
今後はNMUR1発現細胞を同定し、NMUによる刺激で下流シグナルが変化するか、さらにはNMUR1アンタゴニストの投与でシグナルが抑制されるかを検討し、最終的には新たな治療薬の開発につながられればと考えています。